Enzyme là một chất xúc tác sinh học có bản chất là protein, có khả năng tham gia các phản ứng hoá học trong và ngoài cơ thể. Trong bài chỉ đề cập đến enzyme thủy phân.
Enzyme thủy phân có đầy đủ các đặc điểm của một chất xúc tác. Điểm khác nhau của enzyme này so với các xúc tác khác là khả năng xúc tác đặc hiệu và cường lực xúc tác mạnh hơn nhiều so với các xúc tác thông thường. Trong 2 giờ, 1g pepxin thủy phân đến 5kg protein trứng luộc ở nhiệt độ bình thường. Sỡ dĩ phản ứng enzyme diễn ra nhanh như vậy là do năng lượng hoạt hoá trong phản ứng enzyme được hạ xuống rất thấp so với trường hợp không có xúc tác và cũng nhỏ hơn rất nhiều so với các xúc tác khác. Vì có tính đặc hiệu cao nên phản ứng thủy phân của enzyme ít tạo thành sản phẩm phụ có thể gây độc cho người sử dụng.
Bản chất của enzyme là protein nên enzyme cũng có các tính chất tương tự như một protein. Các tác nhân gây biến tính protein như nhiệt độ, acid, kiềm, tác động cơ học… đều có thể làm enzyme biến tính thuận nghịch hoặc không thuận nghịch. Enzyme khác các protein ở chỗ: trong cấu tạo của enzyme một cấu trúc rất đặc biệt gọi là trung tâm hoạt động. Không phải tất cả các phần của enzyme đều tham gia vào hoạt động xúc tác mà chỉ có trung tâm hoạt động mang tính đặc hiệu trong phân tử enzyme mới tham gia xúc tác phản ứng.
Đặc điểm của trung tâm hoạt động của enzyme thuỷ phân
Trung tâm hoạt động của các enzyme thủy phân thường không chứa nhóm ngoại mà chứa các acid amine đặc hiệu. Thường là vòng amidazol của histidine và nhóm hydroxyl của một trong số các gốc serine. Các thành phần trong trung tâm hoạt động sẽ hình thành liên kết yếu để cơ chất có thể gắn vào. Cụ thể là nhóm hydroxyl của serine sẽ hình thành liên kết hydro với nguyên tử nitrogen của vòng amidazol. Chính nhờ liên kết yếu cho nên các nhóm chức trong trung tâm hoạt động rất linh động. Khi có sự cảm ứng của cơ chất, theo thuyết enzyme của Koshland, các nhóm chức này sẽ di chuyển, định hướng chính xác để gắn vào.
Đặc điểm của các cơ chất bị enzyme thủy phân
Các cơ chất của enzyme thủy phân thường là các polyme như protein, glucid, lipid, cellulose… các cơ chất này chứa liên kết bị thủy phân do các phân tử tích điện dương tạo nên mà Bernard Pullman và Albert Pullman gọi đó là “liên kết nhị dương”. Ví dụ: liên kết peptide, liên kết glycoside.
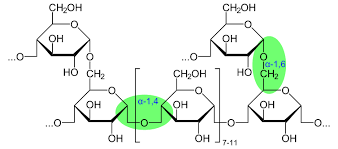
Chính vì vậy, một enzyme muốn thủy phân một cơ chất nào đó, cơ chất đó phải phù hợp về không gian và phù hợp về sự tĩnh điện trong trung tâm hoạt động.
Các yếu tố ảnh hưởng đến hoạt tính xúc tác của enzyme thủy phân
Ảnh hưởng của nhiệt độ
Sự ảnh hưởng của nhiệt độ đến hoạt tính của các enzyme đều theo một quy luật như nhau. Vận tốc xúc tác của enzyme chỉ tăng theo nhiệt độ trong một giới hạn xác định mà ở đó phân tử enzyme chưa bị biến tính. Trong phạm vi nhiệt độ thích hợp, khi nhiệt độ tăng thì hoạt tính của enzyme cũng tăng theo. Khi tăng đến nhiệt độ tới hạn thì hoạt tính xúc tác sẽ giảm và nếu nhiệt độ tiếp tục tăng thì enzyme bị biến tính và mất hoạt tính xúc tác. Thông thường đối với đa số enzyme bị biến tính hoàn toàn ở nhiệt độ lớn hơn hoặc bằng 70oC. Khi nhiệt độ thấp hơn 0oC thì enzyme bị biến tính thuận nghịch và giảm hoạt tính xúc tác hoặc không thể hiện hoạt tính xúc tác.
Mỗi loại enzyme có nhiệt độ tối thích mà tại đó nó thể hiện hoạt tính xúc tác cao nhất. Nhiệt độ thích hợp này phụ thuộc vào loại enzyme, nguồn thu enzyme, pH, kim loại, chất bảo vệ. Thông thường vào khoảng 40 – 50oC.
Ảnh hưởng của pH
pH ảnh hưởng tương tự như nhiệt độ. pH làm thay đổi trạng thái ion hóa của enzyme và cả cơ chất. pH thích hợp cho enzyme hoạt động là giá trị pH mà tại đó enzyme và cơ chất tích điện trái dấu do đó mà kết hợp với nhau dễ dàng.
Đại đa số enzyme thích hợp với pH từ 5 đến 9, nhưng cũng có loại hoạt động ở pH rất thấp (3,5) hoặc rất cao (11). pH thích hợp của mỗi loại enzyme còn phụ thuộc vào nguồn thu enzyme, bản chất enzyme và có thể thay đổi tùy thuộc vào nhiệt độ, cơ chất.
Ảnh hưởng của nồng độ cơ chất và enzyme
Nồng độ cơ chất, enzyme ảnh hưởng lớn đến phản ứng enzyme. Khi cơ chất còn thừa, nếu nồng độ enzyme tăng thì vận tốc phản ứng tăng. Khi hết cơ chất, nếu tăng nồng độ enzyme vận tốc phản ứng vẫn không tăng.
Khi nồng độ cơ chất giảm thì mức độ tiếp xúc giữa enzyme và cơ chất giảm nên phản ứng enzyme cũng giảm.
Khi tăng lượng chế phẩm enzyme sử dụng thì phản ứng thủy phân xảy ra nhanh hơn, đồng thời, lượng sản phẩm tạo thành cũng nhiều hơn.
Ảnh hưởng của chất hoạt hóa và ức chế
Chất hoạt hóa là chất khi thêm vào phản ứng enzyme sẽ làm tăng hoạt tính xúc tác của enzyme hoặc chuyển enzyme từ dạng không hoạt động sang dạng hoạt động. Do vậy khi có mặt chất hoạt hóa vận tốc phản ứng enzyme tăng.
Chất ức chế khi có mặt trong các phản ứng enzyme sẽ làm giảm hoạt tính hoặc mất hoạt tính xúc tác của enzyme. Các chất kìm hãm hoạt động của enzyme thường là các ion kim loại nặng, các phần tử vô cơ, các chất hữu cơ, cũng có thể là các protein và cả cơ chất hay chính sản phẩm của phản ứng.
Tài liệu tham khảo:
1. Nguyễn Đức Lượng, Công nghệ vi sinh tập 2, NXB Đại học Quốc Gia Tp. Hồ Chí Minh, 2006.
2. Nguyễn Đức Lượng et al, Công nghệ enzyme, NXB Đại học Quốc Gia Tp. Hồ Chí Minh, 2004.
3. Lê Ngọc Tú et al, Hóa sinh công nghiệp, NXB Khoa học và Kỹ Thuật Hà Nội, 2005.
FOODNK